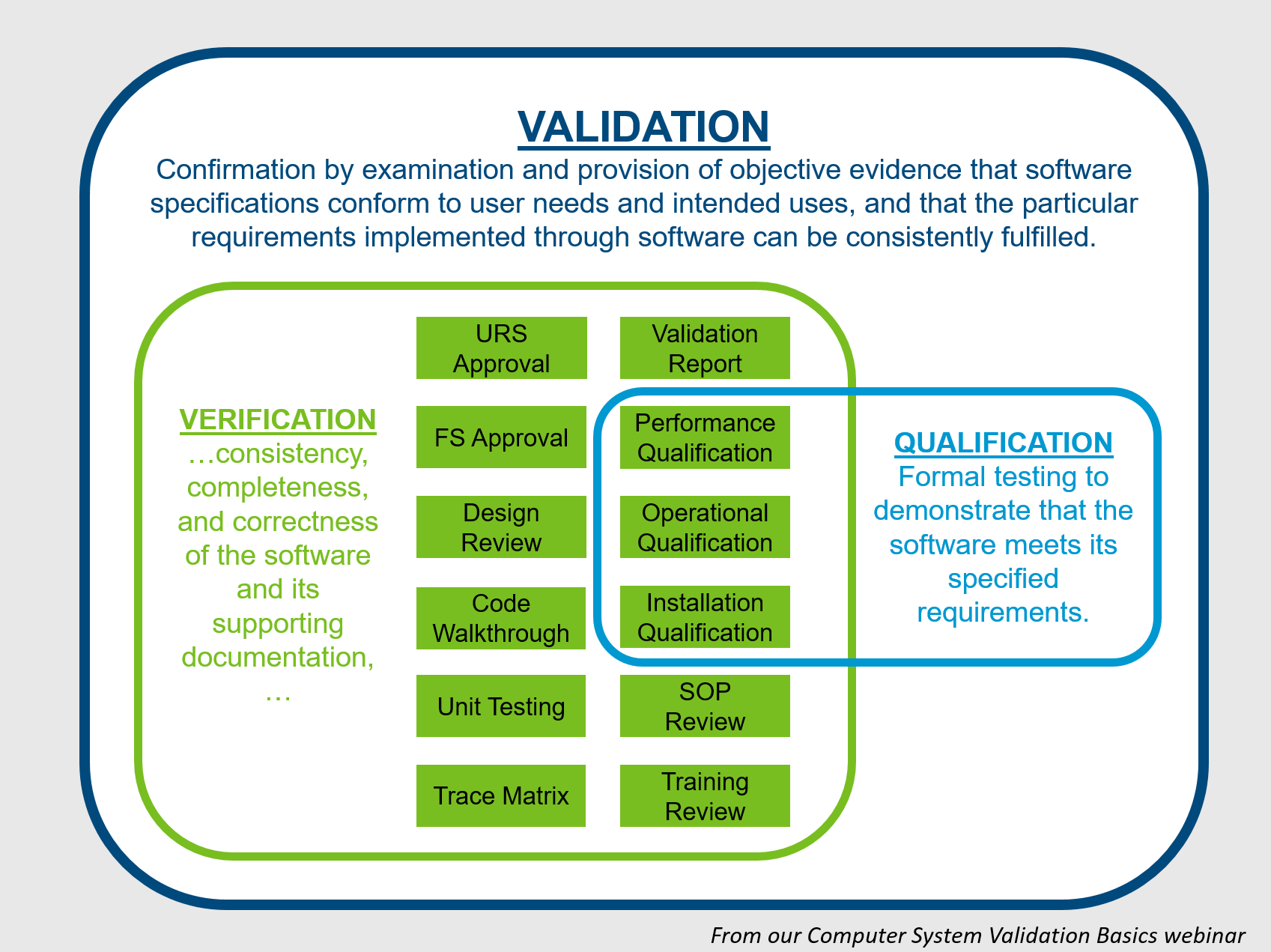
Computer System Validation (CSV): 医薬品業界における必須要件
医薬品業界では、製品の品質や安全性を確保するために、多くの厳しい規制が求められています。その中で、Computer System Validation (CSV)は、コンピュータ化システムが意図した通りに機能し、規制要件を満たしていることを検証するための重要なプロセスです。CSVは単なるソフトウェアのバグチェックにとどまらず、システム全体が正確に機能し、データの整合性や信頼性を保証するための活動です。この記事では、CSVの重要性、対象範囲、実施方法、FDAの規制要件などについて解説します。
Computer System Validation (CSV): その重要性と対象範囲
CSVは、医薬品製造におけるリスク管理の一環として、製品の品質を担保し、患者の安全を守るために欠かせません。医薬品業界では、製造や品質管理の過程で使用されるコンピュータシステムが、その精度と信頼性を欠いた場合、重大な問題を引き起こす可能性があります。CSVを実施することによって、以下の要素に関連するリスクを最小化できます。
1. コンピュータシステム
CSVの対象となるのは、医薬品製造におけるコンピュータ化システム全般です。これには、ハードウェア、ソフトウェア、ネットワークインフラなど、システムを構成する技術的な要素が含まれます。これらの要素が意図した通りに動作し、正常に機能しているかどうかを検証します。
2. 業務プロセス
CSVは、コンピュータシステムだけでなく、実際にそれを利用する業務プロセスにも関連します。業務プロセスとは、システムを使用する手順、標準業務手順書(SOP)、測定機器や記録用具など、医薬品製造のために定められた業務活動全般を指します。これらの要素が正しく連携し、業務フローに沿って動作することを確認することがCSVの目的です。
CSVを実施することで、これらの要素が相互に作用し、全体としての信頼性が確保され、製品の品質や安全性が守られます。
Computer System Validation (CSV): 実施方法とFDA規制
CSVを実施するためには、システム開発ライフサイクル全体を通じて、計画的かつ段階的に検証活動を行う必要があります。特に、米国食品医薬品局(FDA)は、CSVの実施に関する詳細なガイドラインを提供しており、これを遵守することが求められます。CSVは以下のアプローチに基づいて実施されます。
1. ライフサイクルアプローチ
CSVは、システム開発の初期段階からリタイアに至るまで、システムのライフサイクル全体を対象に実施されるべきです。これにより、システムの導入段階から、運用中、そして廃棄に至るまで、適切な検証活動が行われ、継続的にシステムの品質が保証されます。
2. リスクベースアプローチ
FDAでは、CSVにおいてリスクベースアプローチを採用することが推奨されています。これは、システムやプロセスの重要度やリスクレベルに応じて、バリデーションの範囲や厳格さを調整するという考え方です。たとえば、高リスクのシステム(患者の生命に関わる薬剤の製造に関するシステムなど)は、厳格なバリデーションが求められますが、リスクが低い場合には、検証活動を簡素化することが可能です。
3. 文書化
CSVのすべての活動は文書化され、証拠として保管する必要があります。これには、バリデーション計画、テスト結果、変更管理の記録などが含まれます。文書化されたエビデンスは、規制当局による監査の際に求められ、システムの適合性を証明するために重要な役割を果たします。
Computer System Validation (CSV): 製薬企業の責任
CSVの実施において、ソフトウェアのバリデーション作業は外部ベンダーに委託されることもありますが、最終的な責任は製薬企業にあります。FDAは製薬企業に対して、システムの適合性とバリデーションが適切に行われていることを評価し、必要な記録を保管する責任があることを明確にしています。これにより、製薬企業は自社のシステムが規制要件を満たしていることを確認し、万が一の不正操作や不具合が発生した場合でも、その証拠を提出できるように準備しておく必要があります。
Computer System Validation (CSV): 成功のためのポイント
CSVを成功裏に実施するためには、以下のポイントに注意することが重要です。
1. 早期からの計画
CSVはシステム開発の初期段階から計画する必要があります。システム設計や導入の前からバリデーション計画を策定し、早期に検証を始めることで、後の問題を未然に防ぐことができます。
2. 関係者間の協力
CSVは、IT部門、品質保証部門、業務部門など、複数の部門が連携して実施するプロセスです。関係者間での緊密な協力が不可欠であり、各部門が役割分担をしっかりと行いながら進めていく必要があります。
3. 適切なツールと技術の活用
バリデーションのプロセスを効率化するために、適切なツールや自動化技術を導入することが重要です。テストの自動化や、ドキュメント管理ツールを活用することで、作業の精度が向上し、時間やコストの削減が可能となります。
4. 継続的な改善
システムの変更やアップデートが行われるたびに、CSVは見直し、改善されるべきです。新しい技術や規制に対応するために、CSVのプロセスを継続的に改善し、最適な状態を維持することが求められます。
結論
Computer System Validation (CSV)は、医薬品業界にとって欠かせないプロセスです。CSVを適切に実施することで、製品の品質と安全性を保証し、患者を守るとともに、規制要件を満たすことができます。製薬企業は、CSVの重要性を理解し、実施に必要なリソースや計画を確保することで、より安全で信頼性の高い製品を提供することができるのです。
関連文献:
FAQ
CSVはどのような企業に必要ですか?
CSVは特に製薬、医療機器、バイオテクノロジーなどの産業で必要です。
CSVプロセスの最初のステップは何ですか?
CSVプロセスの最初のステップは計画です。
CSVの不備は何を引き起こす可能性がありますか?
不適切なCSVは法的な問題や企業の信用を損なう可能性があります。